Профилактика и лечение острых кишечных инфекций
Поделиться:
Во время купания мы волей-неволей (а маленькие дети даже специально) заглатываем воду вместе с живыми организмами. В подавляющем большинстве случаев такое вторжение остается незамеченным, поскольку наш организм обладает несколькими степенями защиты, помощнее, чем у банковского билета. Но иногда защитная система дает сбой, что провоцирует острую кишечную инфекцию.
Упоминая опасности таящиеся в водоемах, нельзя обойти тему жителей этих водоемов. Речь пойдет о самых опасных существах населяющих наши реки, — пираньях. А, не, шутка — пираньи чуть южнее.
На самом деле мой рассказ, конечно же, о бактериях, о профилактике и лечении кишечных инфекций. Иной раз удивляешься когда мы, такие большие и сильные, обжившие все уголки планеты и даже частичку космоса, погибаем от микроскопических существ. Вспоминается фильм «Война миров» по Уэллсу, где даже самые здоровые инопланетяне спасовали перед микробами.
Впрочем, за инопланетян не поручусь, но людям есть что противопоставить вредным микроорганизмам. В нашей слюне находится вещество (лизоцим), осложняющее жизнь бактерии уже при попадании в рот. Лимфатическое кольцо в ротовой полости, являясь периферическим органом иммунной системы, также надежно защищает от проникновения агрессивных существ. А желудочный сок агрессивен практически к любой флоре. Но при определенных условиях (незрелость иммунной системы у малышей, иммунодефицит, пожилые люди, алкоголики) бактерии берут верх, вызывая острые кишечные инфекции.
Откуда берется инфекция
В водоемах бурлит жизнь, невидимая нашему глазу, и эта жизнь с удовольствием воспользуется телами беспечных купальщиков. Кишечная инфекция — самая обычная проблема летнего сезона. Строго говоря, острая кишечная инфекция возникает не только от купания. Это проблема немытых рук, овощей, фруктов, некачественно обработанной пищи. Причиной кишечной инфекции являются патогенные бактерии (изредка вирусы и грибы).
К слову, в нашем пищеварительном тракте есть и полезные бактерии (бифидобактерии, лактобактерии и др.), иначе говоря, облигатная флора. Они участвуют в пищеварении, выработке ферментов, витаминов, конкурируют с патогенной флорой подавляя ее развитие.
Условно патогенные микроорганизмы (стрептококки, протей, кишечная палочка и пр.), тоже живут внутри организма, и при сохраненном иммунном статусе для нас безвредны. Но способны вызвать заболевание при снижении иммунитета.
А вот бактерии, попадающие извне, — это патогенная флора. Вызванные ими заболевания — иерсиниоз, сальмонеллез, брюшной тиф, холера и т.д. — могут представлять серьезную угрозу жизни.
Как проявляется заболевание
Вначале микробная инвазия проявляется себя… а ничем не проявляет. Инкубационный период длится около двух суток, время, которое есть у пострадавшего, чтобы решить последние дела, пока зловредные микробы множатся, накапливают яды. Дальше интоксикация, температура, ломота в суставах — сутки непонятное состояние, которое можно спутать с гриппом или еще чем-нибудь.
Далее следует расцвет кишечной инфекции. Это, как правило, спастические боли в разных отделах живота, многократная рвота и, конечно, многократный жидкий стул. Иногда жидкость льет как из трубы — как при холере. Иногда с примесью крови — как при дизентерии. Степень обезвоживания достигает крайних величин, угрожая жизни пациента.
Особенно тяжело протекает обезвоживание у маленьких детей. Очень часто таких малышей привозят в наше отделение. Глаза запавшие, крик слабый, кожный покров сухой как ботинок. Тут не до шуток, жизнь висит на волоске.
Факторы, определяющие степень тяжести состояния:
- вид бактерий (от стафиллокока только шестиразовый понос, а от холерного вибриона будет течь как из брандспойта до полного обезвоживания);
- количество бактерий, попавших в организм (от сотни-другой ничего не будет, а вот колония из несколько тысяч особей обязательно вызовет страдание);
- состояние здоровья до инфекционного поражения (здоровый побегает к унитазу и только здоровее станет, а вот сердечнику придется худо).
Вам нужно прекращать заниматься самолечением и травоедением и незамедлительно обратиться к врачу, если: — Вышеперечисленные симптомы наблюдаются у детей дошкольного возраста, пожилых людей старше 60 лет и у лиц с хроническими заболеваниями сердечно-сосудистой и дыхательной систем. — Частый, жидкий стул более 5 раз у взрослых. — В стуле, рвотных массах — примесь крови. — Высокая лихорадка с диареей и рвотой. — Схваткообразные боли в животе любой локализации, длящиеся более часа. — Рвота после любого приема пищи и воды. — Выраженная слабость и жажда.
Что делать в домашних условиях?
- Прежде всего необходимо восполнить обезвоживание. Питье — вот что вам нужно! Если вы не можете восполнить обезвоживание этим методом (возникает рвота, позывы на рвоту), вызывайте скорую. Сколько нужно пить? До тех пор пока жажда не отступит. Всё просто — пейте пока хотите. Риск перегрузить себя жидкостью минимален. Если у вас сопутствующая патология почек, сердца, вызывайте скорую! Пейте чистую, бутилированную воду. Можно восполнять жидкость раствором регидрона — правда, он противен до жути, но полезен микроэлементами.
- Энтеросорбенты. Активированный уголь, энтереодез и всякие подобные невкусные, но полезные и безопасные препараты.
- Если врача нереально вызвать, а рвота усугубляет обезвоживание, найдите церукал (метоклопромид).
- Лекарства при кишечных расстройствах будут нужны, если болезнь не отступает, — понадобятся антибактериальные препараты: бактерию необходимо убить. Выбор препаратов зависит от возможного возбудителя, тяжести состояния, срочности ситуации, аллергии у данного больного. Поэтому «самоназначение» лекарств — не лучшая идея. Но если у вас нет возможности обратиться к врачу, в трудной ситуации (поход, турпоездка) оптимальнее всего — фуразолидон. Его-то и можно держать в аптечке. Принимать по 0,1–0,15 г после еды, 4 раза в сутки для взрослых. Для детей — 10 мг/кг массы тела в сутки (суточную дозу распределяют на 3-4 приема). Принимать не более 10 дней.
- Про еду. В остром периоде лучше не кушать, а пить, пить, пить. Когда станет чуть легче, то можно нежирные бульоны, сухарики. А острый период надо потерпеть.
- При болях в животе обезболивающие лучше не принимать — не стирайте картину заболевания, вдруг аппендицит!
- При диарее нельзя принимать вяжущие средства, вроде имодиума, лоперамида, — организм должен избавляться от токсинов и бактерий.
И в заключение, пусть это банально, повторюсь: мойте руки перед едой, мойте овощи и фрукты, готовьте пищу из качественных продуктов. Это так просто, но необычайно эффективно. Будьте здоровы.
Товары по теме: [product](регидрон), [product](активированный уголь), [product](энтереодез), [product](церукал), [product](фуразолидон), [product](имодиум), [product](лоперамид)
Источник
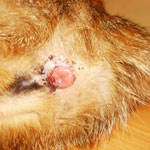
Геморрой у кошек
Причины. Как и у человека, при геморрое у кошек в основе заболевания лежат нарушения регуляции притока и оттока крови в кавернозных венах прямой кишки, приводящие к застою в них крови. Данному заболеванию у кошек способствуют :
- Частые запоры и неправильное питание (кормление кошки сухими кормами при недостаточном поступлении жидкости в организм).
- Отсутствие или наоборот, большие физические нагрузки.
- Ожирение, которое в результате повышенного содержания холестерина в крови вызывает образование бляшек на стенках вен, а иногда и закупорку вен.
- Изменение тонуса кровеносных сосудов и нарушение свойств крови(повышенная вязкость).
- Сбои в работе гормональной системы. Сахарный диабет повышенным содержанием глюкозы в крови оказывает негативное влияние на стенки кровеносных сосудов.
Симптомы. Симптоматика геморроя у кошки сходна с геморроем у человека. При внимательном наблюдении за кошкой владельцы отмечают — кошка начинает ходить широко расставляя задние лапы, стремится как можно реже ходить в туалет. При посещении лотка жалобно мяукает.
Ветеринарный специалист при клиническом осмотре такой кошки методом пальпации в области прямой кишки на начальной стадии регистрирует плотный шар. В дальнейшее этот шар увеличивается в размере и выпячивается за пределы анального отверстии в виде конуса (геморроидальный узел). Если владельцы на этой стадии не обратятся в ветеринарную клинику и не начнут своевременно лечить, то на выпадающем узле в результате постоянной травматизации появятся кровоточащие язвочки. Дополнительно ветеринарный специалист при клиническом осмотре у кошки находит припухлость и покраснение в области анального кольца, отмечает появление геморроидальных узлов. Владельцы кошки при геморрое отмечают сухой кал или длительные запоры. В каловых массах после посещения кошкой лотка находят капельки крови. Поведение кошки становится беспокойным, кошка часто вылизывает область промежности. Течение болезни длительное, с периодическими обострениями, вплоть до выраженной анемии и гнойного воспаления, тромбоза и некроза геморроидальных узлов.
Диагноз на геморрой у кошки ставится на основании проведенного клинического осмотра ветеринарным специалистом. В ветеринарной клинике Вашему питомцу проверят скорость свертывания крови, сделав коагуллограмму, определят уровень гормонов и сахара в крови.
Дифференциальный диагноз. Геморрой у кошки необходимо дифференцировать от воспаления анальных желез и выпадения прямой кишки.
У кошки в области ануса имеются две анальные железы, из которых выделяется секрет, которым кошка метит свою территорию, дополнительно данный секрет оказывает антисептическое действие после акта дефекации. Во время закупорки выводящих протоков образуются абсцессы, которые разрываются и дают кровотечение из ануса.
Выпадение прямой кишки бывает у кошки при тяжелых родах и частых поносах (выпадение прямой кишки у кошки).
Лечение. На начальной стадии заболевания владельцы кошки могут обойтись домашним лечением растительными препаратами. Как и при других заболеваниях желудочно-кишечного тракта у кошек, прежде чем приступить к лечению, необходимо сбалансировать рацион кормления. Еда, которую будет употреблять Ваша кошка в период лечения, должна быть легкоусвояемой, богатой клетчаткой и пищевыми волокнами – они помогают кошке формировать каловые массы и облегчают акт дефекации в лотке. Усилить контроль за потреблением кошкой воды. На период лечение необходимо в рацион кормления ввести кисломолочные продукты.
Лечение при легкой стадии геморроя состоит в гигиеническом уходе за промежностью. Необходимо мыть задний проход кошки 2-3 раза в день теплой водой без мыла, можно использовать влажные салфетки для протирания. После данных процедур область сфинктера необходимо смазывать вазелиновым маслом или антисептическими мазями (левомиколь и др.). При легкой стадии течения геморроя применяют антисептические свечи с ихтиолом, фурозолидоном, лекарственные препараты повышающие тонус вен и сосудов. Из лекарственных трав нашел применение настой тысячелистника, который обладает противовоспалительным, обезболивающим, тромборассасывающим и антисептическим действием.
При переходе геморроя в тяжелую форму (крупные изъязвленные узлы), Вам придется за лечением обращаться в ветеринарную клинику, где хирург с зависимости от особенностей процесса применит одну из двух видов операций:
- Замораживание жидким азотом геморроидальных образований, с последующим их удалением.
- Хирургическое иссечение путем удаления расширенных вен и прилежащей к ним слизистой.
После проведенной операции владельцы должны ограничить кошке ее активность, провести курс витаминизации. Для заживления раневой поверхности применять ранозаживляющие мази (раносан, ируксоветин), а также препараты способствующие ускорению восстановления слизистой оболочки прямой кишки (гамавит, цамакс).
Прогноз. Как правило — благоприятный.
Профилактика. Профилактика геморроя у кошек должна строиться на устранение причин геморроя. При длительных запорах и поносах своевременно обращаться в ветеринарную клинику. Регулярно следить за полноценным кормлением и питьевым режимом. При кормлении необходимо чередовать сухие и мягкие корма, в рацион кормления включать витамины, минеральные корма и комплекс жирных кислот. Регулярно проводить профилактическую дегельминтизацию (глисты у кошек). При увеличение веса у кошки необходима соответствующая диета и физические нагрузки. При неудовлетворительной со стороны кошки гигиены заднего прохода, Вам периодически необходимо будет очищать область заднего прохода с помощью салфеток.
Источник
БОЛЕЗНЬ КОШАЧЬЕЙ ЦАРАПИНЫ
Несмотря на то что первое клиническое описание болезни кошачьей царапины (БКЦ) было дано R. Debre и соавт. более 50 лет назад, до сих пор вопрос об этиологии этого заболевания остается предметом дискуссий и специальных исследований.
Несмотря на то что первое клиническое описание болезни кошачьей царапины (БКЦ) было дано R. Debre и соавт. более 50 лет назад, до сих пор вопрос об этиологии этого заболевания остается предметом дискуссий и специальных исследований. Поскольку выделить возбудитель от больных не удавалось в течение длительного времени, первоначально предполагалась вирусная или хламидийная этиология заболевания. Первые убедительные сведения об идентификации возбудителя БКЦ были получены только в 1983 г., когда исследователи, используя метод окраски по Warthin-Starry (метод серебрения), обнаружили в ткани пораженных лимфатических узлов у 29 из 34 больных БКЦ мелкие полиморфные грамотрицательные бациллы, которые удалось культивировать лишь в 1988 г. Именно этот микроорганизм первоначально был признан возбудителем БКЦ и получил название Alipia felis.
Тем не менее многочисленные последующие исследования не подтвердили четкой взаимосвязи развития БКЦ с A. felis: в большинстве случаев у больных в пораженных тканях не только не обнаруживался указанный возбудитель, но и в сыворотке крови не выявлялись антитела к нему. Более того, из ткани пораженных лимфоузлов был изолирован еще один возбудитель — Bartonella henselae. Методом ПЦР с применением специфических праймеров к Bartonella spp. и A. felis у больных, у которых кожный тест на БКЦ оказался положительным, было установлено, что в 96% случаев у них обнаруживалась ДНК Bartonella, тогда как ДНК A. felis не выявлялась ни в одном случае (A. Bergmans et al., 1995). Сходные данные, подтверждающие ключевую роль B. henselae в развитии БКЦ, были получены и другими исследователями при использовании непрямой реакции флюоресцирующих антител.
В то же время первоначальный факт обнаружения A. felis в пораженных лимфатических узлах игнорироваться не должен. На сегодняшний день некоторые исследователи допускают, что A. felis способен вызывать заболевание, которое по своей клинической картине может напоминать БКЦ.
Болезнь кошачьей царапины (лимфоретикулез доброкачественный) относится к группе бартонеллезов и характеризуется как нетяжелое самокупирующееся заболевание с развитием одностороннего лимфаденита, регионарного по отношению к месту инокуляции возбудителя, и только в редких случаях возможна диссеминация возбудителя с поражением центральной нервной системы и висцеральных органов.
B. henselae характеризуется как небольшая плеоморфная, грамотрицательная бацилла, весьма требовательная к условиям культивирования (растет только на средах с 5% кровяного агара при температуре от 35 до 37°С, с 5—10% углекислого газа и 40-процентной влажностью). Кроме этого, колонии первичной культуры растут медленно и становятся видимыми только после 9—15 дней роста. При последующем пассаже рост колоний ускоряется. Идентификация выделенного возбудителя проводится с использованием специфических антисывороток, определением профиля жирных кислот клеточной стенки или молекулярно-генетическим методом. С помощью этого метода было идентифицировано два генотипа B. henselae, хотя до сих пор четкой зависимости между генотипами возбудителя и особенностями клинического течения вызываемых ими заболеваний не установлено.
B. henselae на сегодняшний день рассматривается как основной возбудитель БКЦ, однако у 5—15% больных с диагнозом, установленным на основании клинико-эпидемиологических данных, даже с помощью существующих современных методов лабораторной диагностики этиологическое значение B. henselae в развитии заболевания не подтверждается.
Один из необъяснимых парадоксов, связанных с B. henselae: в последние годы установлено, что данный возбудитель ответственен за развитие не только БКЦ, но и некоторых других заболеваний.
БКЦ имеет широкое географическое распространение и встречается практически повсеместно. Основным естественным резервуаром B. henselae являются кошки, инфицированность которых в значительной степени определяет распространенность БКЦ (K. M. Zangwill et al., 1993). По данным некоторых исследователей, у более чем 50% домашних и диких кошек обнаруживается бактериемия, обусловленная B. henselae. В ходе исследования, проведенного в США, установлено, что наиболее высокий процент инфицированности кошек и, соответственно, заболеваемости БКЦ среди людей регистрируется в южных штатах. Большинство исследователей подчеркивают особую роль котят в передаче возбудителя, указывая, что у взрослых кошек редко выявляется бактериемия B. henselae за счет наличия у них специфических антител, свидетельствующих о длительности их инфицирования. Особенностью течения бартонеллеза у кошек является его продолжительность (месяцы, годы) и бессимптомность (даже в случае подтверждаемой бактериемии).
В циркуляции B. henselae среди кошек исключительную роль играют блохи (Ctenocephalides felis). Экспериментальным путем было установлено, что при отсутствии блох инфицирования здоровых кошек не происходит.
B. henselae обнаруживается в кишечнике блох и их испражнениях в течение 9 дней после инфицирования, что свидетельствует о его репликации и персистенции в организме блох. Кроме этого, экспериментально была установлена возможность инфицирования кошек путем внутрикожной инокуляции инфицированных испражнений блох, в то же время оральное введение кошкам инфицированных блох и их испражнений к сероконверсии не приводило. Роль блох в передаче возбудителя от кошек к человеку в настоящее время категорически не отрицается. В последние годы исследователями в США и Италии (Y. O. Sanogo et al., 2003) молекулярно-генетическими методами было продемонстрировано, что ДНК B. henselae может обнаруживаться в иксодовых клещах, хотя их роль в качестве вектора передачи возбудителя БКЦ по-прежнему не изучена.
«Травматический» контакт с кошками (царапины, укусы) весьма характерен для БКЦ и отмечается более чем у 90% заболевших. Установлено, что «резервуаром» B. henselae могут быть и собаки, однако достоверно подтвержденных случаев заражения от них людей пока не описано.
Эпидемиологические исследования показывают, что в сыворотке крови около 20% владельцев кошек и 3–4% общей популяции людей обнаруживаются антитела к B. henselae. Семейные случаи заболевания БКЦ не столь типичны и регистрируются менее чем у 5% пациентов. Хотя БКЦ может развиваться в любом возрасте, чаще заболевают молодые люди (до 18 лет).
Передача возбудителя БКЦ реализуется главным образом контактным путем через царапины, укусы или слюну инфицированных кошек. Подъем заболеваемости, как правило, отмечается с конца лета, что объясняется особенностями жизненного цикла у кошек и блох.
Поскольку возбудитель БКЦ был идентифицирован относительно недавно, многие аспекты, касающиеся патогенеза заболевания, до сих пор недостаточно изучены. Характер развивающегося инфекционного процесса, обусловленного действием B. henselae, в значительной степени зависит от иммунного статуса человека: в тех случаях, когда заболевание развивается у иммунокомпетентных пациентов, диссеминация возбудителя отсутствует, и процесс преимущественно ограничивается локальными или регионарными поражениями. В частности, БКЦ в большинстве случаев проявляется развитием регионарной лимфаденопатии. Поражение висцеральных органов описано только в отдельных случаях (Dunn et al., 1997), а бактериемия у иммунокомпетентных пациентов регистрируется исключительно редко (Slater et al., 1990). Напротив, у иммунокомпрометированных пациентов для инфекции B. henselae типично развитие бактериемии и других системных поражений, включая бациллярный ангиоматоз и бациллярный пелиозный гепатит, а у лиц с врожденными и приобретенными аномалиями клапанов сердца — эндокардит (Raoult et al., 1996).
Гистологические изменения в пораженных лимфатических узлах характеризуются пролиферацией гистиоцитов и B-лимфоцитов, приводящей к образованию гранулем с последующей нейтрофильной инфильтрацией и развитием центрального или звездчатого некроза.
Хотя B. henselae и считается одним из наиболее вероятных возбудителей БКЦ, тем не менее, согласно современным наблюдениям, данный возбудитель ответственен за развитие ряда других патологических состояний человека (табл. 1). При этом иммунный статус больных рассматривается как ключевой фактор, определяющий характер формирующегося заболевания, хотя известны случаи, когда даже у лиц с ВИЧ-инфекцией в стадии СПИДа БКЦ протекала в типичной форме.
 |
| Таблица 1. Заболевания человека, вызываемые B. henselae |
Инкубационный период у больных с БКЦ может варьировать в достаточно широких пределах — от 3 до 20 дней и более, составляя в среднем 1–2 нед. Хотя общепринятой клинической классификации БКЦ нет, чаще всего выделяют типичную и атипичные формы заболевания (табл. 2), что определяется по доминирующему в клинической картине болезни синдромокомплексу.
В типичных случаях БКЦ проявляется развитием первичного аффекта и регионарного (к месту входных ворот инфекции) лимфаденита. Локализация первичного аффекта определяется местом первичной инокуляции возбудителя, а именно местом нанесения кошкой царапин и укусов. По истечении нескольких дней (от 3 до 10), когда нанесенные кошкой повреждения кожи уже заживают, в месте входных ворот формируется папула, которая, как правило, трансформируется в везикулу и далее в пустулу, а после вскрытия — в язвочку, покрытую корочкой. В некоторых случаях пустула может подсыхать без образования язвочки. В диаметре размер формирующейся папулы, как правило, составляет от 1–2 до 5 мм. Частота выявления первичного аффекта у больных БКЦ, по данным различных исследователей, может колебаться от 25 до 94%. Кожные проявления сохраняются в течение 1—3 нед и спонтанно разрешаются.
Регионарный лимфаденит является одним из наиболее постоянных и характерных клинических признаков БКЦ (табл. 3) и сохраняется в течение длительного времени: от 7 до 60 дней, а в отдельных случаях до 1 года и даже 3 лет. В большинстве случаев лимфаденит разрешается в течение 1—4 мес. Нередко он оказывается практически единственным проявлением БКЦ. В большинстве случаев (85%) у больных выявляются одиночные лимфатические узлы, реже множественные, в границах одной анатомической области. Несмотря на то что у больных регистрируется увеличение лимфатических узлов, осуществляющих дренаж места первичной инокуляции возбудителя, развитие лимфангоита не характерно для БКЦ. У 1/3 пациентов могут определяться увеличенные лимфатические узлы разных анатомических областей, хотя генерализованная лимфаденопатия встречается достаточно редко. Размером увеличенные лимфатические узлы чаще бывают от 1 до 5 см, в некоторых случаях до 8—10 см. При пальпации лимфатические узлы умеренно болезненные. Хотя они и не спаяны с окружающими тканями, нередко определяется гиперемия кожных покровов над ними. В 10—50% случаев у больных БКЦ развивается нагноение пораженных лимфатических узлов с образованием густого желто-зеленого гноя. В отдельных случаях при посеве гноя на питательные среды удается получить рост стафилококков и другой флоры, хотя роль условно-патогенной флоры (суперинфекция) в нагноении пораженных лимфатических узлов пока не установлена.
Общее состояние больных в большинстве случаев остается удовлетворительным. Только в трети случаев у больных отмечается повышение температуры тела свыше 38,3°С, которое сохраняется около недели и лишь иногда может затягиваться до месяца и более. Среди других клинических проявлений БКЦ могут отмечаться: слабость и недомогание (30%), головная боль (14%), тошнота и рвота (15%), спленомегалия (11%). В случае длительного течения заболевания у больных может наблюдаться потеря веса. Нередко заболевание приобретает волнообразное течение.
Поражение глаз (глазной вариант) при БКЦ регистрируется в том случае, когда местом инокуляции возбудителя служит слизистая оболочка глаз. Клинические проявления заболевания в этом случае будут включать развитие одностороннего поражения в виде язвенно-гранулематозного конъюнктивита, отека век и преаурикулярной лимфаденопатии (синдром Парино). Одновременно у больных могут определяться умеренно увеличенные и болезненные околоушные и шейные лимфатические узлы. К числу других глазных проявлений БКЦ относятся нейроретинит, неврит зрительного нерва и папиллит. Для нейроретинита типично одностороннее острое нарушение остроты зрения, развивающееся на фоне умеренно выраженных явлений интоксикации. При осмотре глазного дна могут выявляться геморрагии, множественные дискретные повреждения, ватоподобные образования, отек и экссудация соска зрительного нерва (симптом «макулярной звезды») (J. B. Reed et al., 1998).
Поражение нервной системы (неврологический вариант) у больных БКЦ выявляется редко (
2% случаев), хотя диапазон клинических проявлений весьма разнообразен: у больных могут выявляться радикулиты, полиневриты, миелит, энцефалопатия, энцефалит, менингит и церебральная атаксия. Характерным признаком поражения нервной системы при БКЦ является то, что они развиваются спустя 1—6 нед (чаще 2–3 нед) от момента появления лимфаденопатии. Для развития энцефалита и менингита типично внезапно возникающее ухудшение состояния больного, сопровождающееся лихорадкой, головной болью, спутанностью сознания и дезориентацией. В некоторых случаях состояние может прогрессивно ухудшаться, вплоть до развития комы. В ликворе у таких больных определяется мононуклеарный плеоцитоз. Только в отдельных случаях у больных после перенесенного энцефалита могут отмечаться резидуальные явления.
Некоторые авторы (P. M. Delahoussaye, B. M. Osborne, 1990), указывая на возможность поражения печени и селезенки при БКЦ, выделяют висцеральный вариант заболевания, для которого характерны длительная волнообразная лихорадка, увеличение размеров печени и селезенки, повышение в сыворотке крови уровней аминотрансфераз, с определением при УЗИ и компьютерной томографии множественных, диффузных, гипоэхогенных дефектов. Довольно часто у таких больных отмечается генерализованная лимфаденопатия.
Кроме этого, в более редких случаях у больных БКЦ могут выявляться абсцесс селезенки, плеврит, эндокардит, пневмония, узловатая эритема, тромбоцитопеническая пурпура, остеомиелит (B. Dzelalija et al., 2001, C. V. Hulzebos et al., 1999).
В типичных случаях первичная диагностика БКЦ не представляет больших сложностей, поскольку основывается на характерных клинико-эпидемиологических данных (табл. 4).
Определенные сложности имеются при лабораторной верификации диагноза, что связано с отсутствием соответствующей лабораторной базы. В зарубежной практике длительное время в качестве основного диагностического критерия БКЦ использовался кожный тест, в котором в качестве аллергена применялся термоинактивированный пунктат, полученный из лимфоузлов больных с установленным (в соответствии с принятыми критериями) диагнозом БКЦ. По данным многих авторов, результативность такого теста достигала 95—98%, однако из-за риска передачи гемоконтактных инфекций использование данного теста ограничено, а кожного теста с использованием очищенных антигенов B. henselae пока не описано.
Микробиологические исследования в широкой практике не применяются ввиду длительности (от 2 до 6 нед) и сложности проведения анализа.
Достаточно информативным способом установления диагноза является биопсия папул и/или пораженных лимфатических узлов с последующим гистологическим исследованием (окрашивание срезов гематоксилин-эозином и серебром — метод Warthin-Starry), позволяющим выявить характерные гистологические признаки поражения и скопление мелких плеоморфных бактерий.
В последние годы большое внимание уделяется разработке специфических иммунологических (ИФА) и молекулярно-генетических (идентификация гена 16S рибосомальной РНК B. henselae) методов обнаружения возбудителя БКЦ в биопсийном материале больного, хотя пока для широкой практики они по-прежнему недоступны.
Дифференциальный диагноз необходимо проводить с заболеваниями, сопровождающимися развитием лимфаденопатии (табл. 5).
Несмотря на то что в редких случаях отмечаются варианты тяжелого течения БКЦ, у иммунокомпетентных лиц прогноз заболевания благоприятный. Повторных случаев и летальных исходов не описано.
Многочисленные клинические наблюдения показывают, что в большинстве случаев БКЦ протекает как самокупирующаяся инфекция, и применение антибактериальной терапии не оказывает существенного влияния на ее течение. Традиционные рекомендации по применению эритромицина (эритромицин-тева, зинерит) и доксициклина (юнидокс солютаб, медомицин, вибрамицин, тетрадокс) основаны на эффективности этих препаратов у больных с ВИЧ-инфекцией при развитии бациллярного ангиоматоза, вызываемого Bartonella quintana, тогда как у больных БКЦ терапевтическая эффективность указанных препаратов не подтверждена ни в одном исследовании. Весьма противоречивыми остаются данные по соответствию чувствительности in vitro возбудителя БКЦ к антибактериальным препаратам и их клинической эффективности. Единственным антибактериальным препаратом, клиническая эффективность которого была установлена в ходе рандомизированного плацебо-контролируемого исследования, является азитромицин (сумамед, хемомицин, азивок, сумазид), назначаемый в течение 5—10 дней. В неконтролируемых исследованиях (A. M. Margileth, 1992) из 18 антимикробных препаратов клиническая эффективность была установлена только при применении рифампицина (бенемицин, р-цин), ципрофлоксацина (ципросан, цифран, ципрова), гентамицина (гентамицин К, гентамицина сульфат) и триметопримсульфаметоксазола (бактрим, септрин). Антибактериальные препараты при БКЦ следует применять у иммунокомпрометированных лиц и при тяжелом течении заболевания, сопровождающегося поражением нервной системы и висцеральных органов.
В случае выявления флуктуации в пораженном лимфатическом узле требуется его пункция и аспирация гноя, что ускоряет последующий процесс склерозирования и рубцевания ткани лимфатического узла и влияет в конечном итоге на выздоровление пациента.
По вопросам литературы обращайтесь в редакцию.
В. А. Малов, доктор медицинских наук, профессор
А. Н. Горобченко, кандидат медицинских наук, доцент
ММА им. И. М. Сеченова, Москва
Источник




