- Оценка расширения и сужения каудальной полой вены у собак и кошек методами рентгенографической диагностики
- Полезно знать
- Портосистемные шунты у собак и кошек. Топология портосистемных шунтов (по данным компьютерной томографии)
- К какому разделу относят данную патологию
- У кого встречается эта патология
- Клинические проявления
- Рентгенография
- Топология портосистемных шунтов
- Видео
Оценка расширения и сужения каудальной полой вены у собак и кошек методами рентгенографической диагностики
Болезни кардиального и респираторного тракта у собак и кошек, а также других видов домашних жывотных имеют достаточно высокую инцидентность. Болезни, которые сопровождаются развитием застойной сердечно-сосудистой системы достаточно вариабельны. Течение и формы болезни сердечно-сосудистой системы у собак и кошек также имеюют существенную вариабельность. В ряде случаев у живортных развиваеся недостаточность правых камер сердца, которая сопровождается застоными явлениями в большом круге кровообращения.
Как мы уже рассматривали в предыдущих статьях, в боковых и прямых проекциях рентгеновских снимков могут проявляться симптомы застойной правожелудочковой недостаточности:
- увеличение тени правого предсердия
- увеличение тени правого желудочка
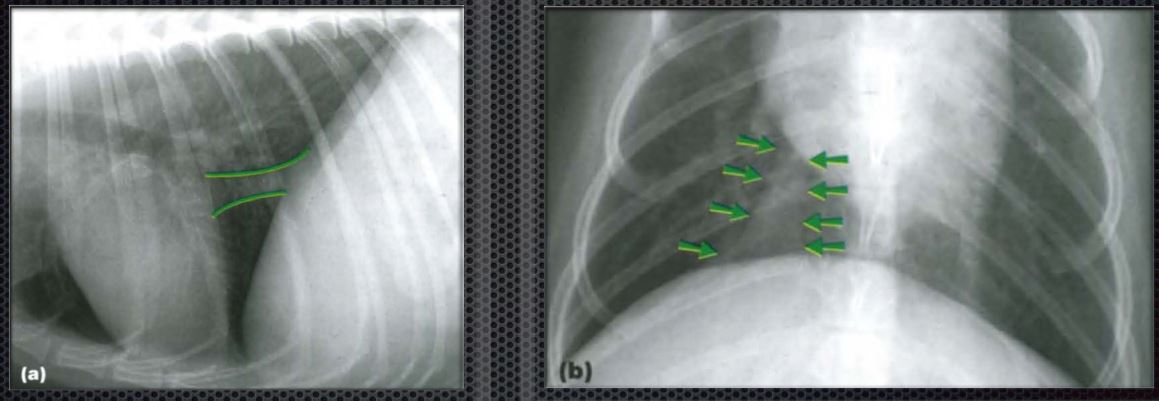
Кроме указанных изменений при рентгендиагностике собак и кошек, больных застойной правожелудочковой недостаточностью, можно выявить расширение каудальной полой вены.
Следует отметить, что размер каудальной полой вены может вариировать в зависимость от фазы сердечного и дыхательного цикла.
Имеются критерии нормального размера каудальной полой вены у мелких домашних животных. Клинически значимое расширение каудальной полой вены выявляют в тех случаях, когда ее диаметр превышает длину тела 5-7 грудного позвонка. Диаметр каудальной полой вены при этом выполняют на рентеновских снимках, выполненных правой боковой проекции.
Существует также другой способ диагностики расширения каудальной полой вены путем сравнения ее размера с рамером нисходящей аорты, которая также является важнейшим магистральным сосудом и достаточно хорошо визуализируется на рентгеновских снимках.
Дилатацию каудальной полой вены считают доказанной и клинически значимой, если ее размер в 1,5 раза превышает размер нисходящей аорты.
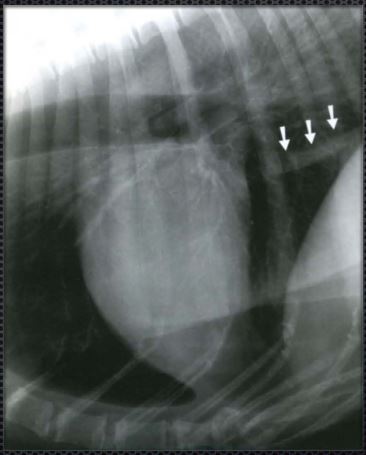
В ряде случаев можно выявить сужение каудальной полой вены. Данный рентгенографический симптом выявлется при резкой гиповолемии:
- гиповолемический шок
- геморрагический шок
Диаметр каудальной полой вены в таких случаях может быть меньшим нежели 1/2 размера нисходящей части аорты или размера тела 5-7 грудного позвонка.
Таким образом, размер каудальной полой вены у собак и кошек — это важный параметр инструментальной диагностики и должен определяться при стандартном рентгенологическом исследовании сердечно-сосудистой системы.
Полезно знать
© VetConsult+, 2016. Все права защищены. Использование любых материалов, размещённых на сайте, разрешается при условии ссылки на ресурс. При копировании либо частичном использовании материалов со страниц сайта обязательно размещать прямую открытую для поисковых систем гиперссылку, расположенную в подзаголовке или в первом абзаце статьи.
Источник
Портосистемные шунты у собак и кошек. Топология портосистемных шунтов (по данным компьютерной томографии)
К какому разделу относят данную патологию
Как образуется портосистемный шунт. Врождённые и приобретённые шунты
Кровообращение плода (рис.2) отличается от кровообращения взрослого животного. Артериальная кровь от плаценты к плоду идёт по пупочной вене. В воротах печени пупочная вена разделяется на две ветви: первая ветвь впадает в воротную вену, а вторая ветвь (венозный проток)— в одну из печеночных вен или в каудальную полую вену. Таким образом, артериальная кровь, которая оттекает по пупочной вене от плаценты, частично поступает непосредственно в нижнюю полую вену, а частично — в печень, являющуюся у плода органом кроветворения. То есть, существование у эмбриона сосудов, по которым кровь из воротной вены сбрасывается в каудальную полую или непарную вену, является нормой.
Считается, что дополнительные сосуды, шунтирующие у плода воротную кровь в обход печени, могут располагаться и вне печени.
В норме в первые дни после рождения животного сосуды, шунтирующие печень, должны закрыться и воротная вена должна стать самостоятельным сосудом, не связанным с системными венами. Если эмбриональные сосуды, шунтирующие печень не закрылись, то с началом полноценной работы желудочно-кишечного тракта и повышением давления в воротной вене они становятся врождёнными портосистемными шунтами (рис. 3, 4).
У взрослого животного с патологией печени, вызывающей повышение давления в воротной вене, закрывшиеся и полностью запустевшие эмбриональные сосуды, могут постепенно восстановить свою функцию и стать приобретёнными (вторичными, по отношению к первичной печёночной патологии) шунтами. Приобретённые шунты часто могут быть множественными.
У кого встречается эта патология
Клинические проявления
Лабораторная диагностика
Визуальная диагностика
Рентгенография
На обзорных рентгенограммах брюшной полости ищут последствия наличия шунта: уменьшение размеров тени печени, тени рентгеноконтрастных камней в почках и мочевом пузыре. Кристаллы урата аммония не рентгеноконтрастны, но нередко при портосистемных шунтах образуются камни более сложного состава, являющиеся рентгеноконтрастными (рис. 5, 6) .
Для визуализации воротной вены и шунта применяют селективную ангиографию воротной вены– портографию.
Существует несколько методик портографии:
- введение рентгеноконтрастного вещества в брыжеечную вену;
- введение рентгеноконтрастного вещества в сосуды селезёнки;
- введение рентгеноконтрастного препарата в краниальную брыжеечную артерию.
Каждый из методов обладает своими плюсами и минусами. Введение рентгеноконтрастного вещества в брыжеечную вену подразумевает проведение лапаротомии, что достаточно трудоёмко и связано с рисками, сопутствующими подобным операциям. Введение контрастного препарата в сосуды селезёнки связано с пункцией селезёнки под контролем УЗИ, а в брыжеечную артерию требует катетеризации бедренной артерии.
Топология портосистемных шунтов
Внепечёночный шунт может полностью располагаться за пределами печени, начинаясь от одного из притоков воротной вены (обычно от селезёночной вены или левой желудочной) и впадая в каудальную полую, диафрагмальную или непарную вену (рис. 10).
Приобретённый шунт чаще начинается от селезёночной вены и впадает в левую почечную вену или в левую яичниковую (семенниковую), которая в свою очередь впадает в левую почечную вену (рис. 11).
Шунт может быть множественным (несколько шунтов), может иметь дополнительные петли.
Сосудистое русло животного может отличаться от стандартного, описанного в учебниках. Это не патология, а вариант нормы. При наличии шунта крайне важно описать анатомические варианты хода основных сосудов (рис. 12).
КТ-ангиография позволяет не только обнаружить шунт, но и всесторонне описать его топологию: исследовать между какими сосудами происходит сброс крови, описать локализацию шунта, оценить его размеры, выявить наличие множественных шунтов, описать другие особенности сосудистого русла исследуемого пациента.
Источник
Видео
Клинический случай стеноза мочеточника у кота при аномалии развития каудальной полой вены

Еще фото
Автор (ы): А.Н. Лапшин, Ветеринарный врач-хирург, Ветеринарная клиника неврологии, травматологии и интенсивной терапии, Санкт-Петербург, Кафедра анатомии и гистологии МГАВМиБ им. К.И. Скрябина, Москва / A. Lapshin, DVM, Veterinary Clinic of Neorology, Traumatology and Intensive Therapy, St.-Petersburg, Faculty anatomy and histology of the Moscow State academy of Veterinary Medicine and Biotechnology named K.I. Skryabin
Журнал: №1 — 2016
Ключевые слова: ретрокавальный мочеточник, аномалия каудальной полой вены, субкутанный нефровезикулярный шунт
Key Words: retrocaval ureter, caudal vein anomaly, subcutaneous ureter bypass
Сокращения: РМ – ретрокавальный мочеточник, КПВ – каудальная полая вена, СНШ – субкутанное нефровезикулярное шунтирование
Аннотация: Ретрокавальный мочеточник встречается довольно редко в клинической практике. стеноз мочеточника является результатом аномалии развития полой вены, при которой происходит латерализация каудальной полой вены и дорсальное положение мочеточника относительно ее. мы используем субкутанный нефровезикулярный шунт для лечения в данном случае.
Summary: Retrocaval ureter is rare clinical condition in clinical practice. Ureter stenosis is one of the result of the vena cava anomaly, because lateralization of the vena cava and dorsal position of the ureter against the vine cava. We use subcutaneous ureter bypass devise for treatment in this case.
Введение
Одной из не ятрогенных причин развития стеноза мочеточника у молодых котов может быть аномалия развития каудальной полой вены, при которой последняя смещена в сторону или имеет дубликатуру. В клинической практике данное сочетание патологий называется ретрокавальный, или циркумкавальный мочеточник. Правая каудальная кардинальная вена в норме обеспечивает адекватное кровоснабжение у плода, но после рождения редуцируется. В результате нарушения этого процесса сохраняющаяся кардинальная вена смещает мочеточник и формирует ретрокавальный мочеточник, т. е. мочеточник вместо нормального расположения относительно каудальной полой вены огибает ее дорсально (рис. 1, 2).
Наиболее часто ретрокавальный мочеточник выявляется справа, что связано с особенностью анатомического строения и близости правого мочеточника и правой каудальной кардинальной вены. Ретрокавальный мочеточник с левой стороны редко встречается. В гуманной медицине наиболее часто левосторонний ретрокавальный мочеточник выявляется при situs inversus, т.е. при врожденной транспозиции внутренних органов. В ветеринарной медицине левосторонний ретрокавальный мочеточник был описан Doust R.T. у собаки породы бернский зенненхунд с правосторонним внутрипеченочным шунтом.
Описание клинического случая
В клинику из другого ветеринарного учреждения был направлен 2-летний кастрированный кот породы курильский бобтейл с пиелоэктазией правой почки и признаками обструкции мочеточника в верхней трети. Из общения с владельцем животного стало известно, что в течение 2 последних месяцев у кота отмечается макрогематурия, затрудненное мочеиспускание и положительная динамика на фоне терапии цистита неясной этиологии. При контрольном ультразвуковом исследовании мочевыделительной системы было подтверждено наличие выраженной пиелоэктазии правой почки до 24 мм. Биохимическое исследование крови не выявило азотемии, и общее состояние пациента было удовлетворительным. При тесте на хронические вирусные инфекции у пациента было подтверждено носительство вируса лейкемии кошек (FeLV). Было принято решение о проведении диагностической лапаротомии и ряда контрастных исследований для определения причины обструкции правого мочеточника.
Под общей анестезией с соблюдением принципов асептики и антисептики проведена диагностическая лапаротомия. В результате было обнаружено два утолщения стенки правого мочеточника в средней и нижней частях. При пальпации данных участков мочеточника признаков наличия конкрементов в них выявлено не было. Выполнена уретеротомия и биопсия стенки мочеточника по средней части в области первого утолщения. В уретеротомную рану в ретроградной манере введен катетер и выполнена антеградная пиелография (рис. 3). В верхней трети мочеточника выявлен участок стеноза мочеточника с зонами пред- и постстенотической дилатации мочеточника. На серии рентгеновских снимков отмечена выраженная пиелоэктазия. При ревизии брюшной полости выявлена латерализация каудальной полой вены и дорсальное положение мочеточника относительно КВП (рис. 4, 4а). Таким образом, интраоперационно был подтвержден ретрокавальный мочеточник.
Для коррекции данной аномалии принято решение сделать установку субкутанного нефровезикулярного шунта. Для этого провели диссекцию каудального полюса почки на площади 2 см. Под рентгеноскопическим контролем из этой области проводится пиелоцентез и пиелография (рис. 5). По игле в полость лоханки вводится проводник, и с его помощью формируется несколько туров по лоханке. После чего игла удаляется, а проводник остается на месте. По проводнику в полость лоханки вводится первый катетер и с помощью тракционной нити производится формирование pigtail-кончика, что позволяет зафиксировать и заблокировать катетер в лоханке.
Для дополнительной фиксации катетер снабжен специальной дакроновой манжетой, которая прижимается к капсуле почки, и между ней и капсулой вводится цианакрилатовый тканевой клей. Клей позволяет дополнительно зафиксировать катетер в лоханке и обеспечить нужную герметичность в зоне вкола катетера в почку. Кончик катетера выводится в подкожное пространство, где между подкожной жировой клетчаткой и мышцами формируется карман. Второй катетер вводится в мочевой пузырь напрямую через стенку в области верхушки. Для этого первично формируется кисетный шов. Кончик катетера, перфорируя стенку мочевого пузыря по центру кистевого шва, вводится в его полость. Кисетный шов затягивается, и дакроновая манжета катетера подшивается к серозно-мышечной оболочке мочевого пузыря в 4 точках. Все пространство между манжетой и стенкой мочевого пузыря заполняется тканевым клеем. Свободный конец катетера выводится в ранее сформированный карман в подкожном пространстве и соединяется с почечным катетером c помощью порт-системы. Под рентгеноскопической ассистенцией проверяется герметичность всех соединений. Для этого в порт-систему вводится контрастный агент. При интраоперационном контрастном исследовании отмечалось нормальное прохождение контрастного агента в лоханку почки и мочевой пузырь (рис. 6). Рана была закрыта послойно.
В первые сутки после операции у пациента наблюдалось удовлетворительное общее состояние, нормальная активность и аппетит. По данным УЗИ, объем лоханки после шунтирования уменьшился до 6 мм. На вторые сутки после операции при контрольном УЗИ обнаружено увеличение объема лоханки до 28 мм. При рентгенографии был выявлен перегиб почечного катетера (рис. 7). В результате решено было провести хирургическую ревизию и повторное контрастное исследование для подтверждения обструкции почечного катетера. При ревизии обнаружено, что почечный катетер перегнулся в области его входа в брюшную полость через брюшную стенку (рис. 8). Для коррекции обструкции кончик почечного катетера был резецирован и сформирован новый вход в брюшную полость каудальнее, что позволило сформировать большую петлю катетера для профилактики повторного перегиба.
Ранний послеоперационный период прошел без особенностей (рис. 9). Срок отдаленного наблюдения в настоящий момент составляет 245 дней. За этот период пациент поступал 2 раза в клинику на санацию порт-системы и параллельно с этим получал лечение от цистита.
Выводы
Впервые техника нефровезикулярного шунтирования описана в 1994 г. Lingam и соавторами. Концепция создания искусственного соединения между лоханкой почки и полостью мочевого пузыря использована в паллиативной помощи в урологической практике у пациентов с метастатическими поражениями области малого таза, ретроперитонеального пространства и инвазией в мочеточники. Техника рассматривалась как альтернатива нефростомии у подобных пациентов и показала улучшение качества жизни пациентов.
В ветеринарной медицине техника была модернизирована и описана Berent и соавторами в 2010 г. Само устройство для субкутанного нефровезикулярного шунтирования (СНШ) представляет собой 2 полиуретановые перфорированные на концах трубки, первая с кончиком pigtail, а вторая c прямым кончиком, соединяющиеся посредством порт-системы.
В настоящее время, по мнению многих авторов, техника СНШ является наиболее перспективной методикой лечения обструкции мочеточника при уретеролитиазе и стриктуре/стенозе (Berent, Shipov, Segev). Эта методика применяется при невозможности выполнить стентирование мочеточника или неэффективности предыдущего стентирования.
В сравнении со стентированием мочеточника она имеет меньший процент осложнений в лечении уретеролитиаза у кошек.
В практике гуманной медицины ретрокавальные мочеточники субтипируют на группы по анатомической локализации зоны стриктуры мочеточника, т.е. перекрещивание с каудальной полой веной. Тип 1 ретрокавального мочеточника характеризуется поражением средней или дистальной части мочеточника, в то время как тип 2 – высокой петлей в проксимальном отделе мочеточника (Salonia A.). В ветеринарной практике данного разделения не описано. Считается, что РМ может быть выявлен как находка и является бессимптомным в клиническом проявлении. Клинические проявления варьируются, и клиническое состояние может не соответствовать структурным изменениям, выявленным по данным визуальных и лабораторных методов диагностики, несмотря на то, что структурно происходит расширение лоханки из-за недостаточного пассажа мочи по мочеточнику. Общее состояние пациента остается удовлетворительным и ничем не примечательным даже в ситуациях, когда размер лоханки уже превышает 20 мм.
Несмотря на отсутствие явной клинической симптоматики, данных пациентов нельзя назвать бессимптомными. Эпизодическая гематурия и странгурия, которые иногда наблюдаются у пациентов с ретрокавальным мочеточником, не являются патогномоничными для болезни, но требуют от специалиста проведения диагностических мероприятий, при которых и выявляется пиелоэктазия и локальный гидроуретер. По результатам визуальной диагностики можно выявить зону сужения просвета мочеточника при проведении пиелографии или выделительной урографии. При включении РМ в лист дифференциальных диагнозов проведения неселективной каваграфии из 2 бедренных вен, можно определить отклонения от нормы, анатомию строения каудальной полой вены, а именно ее латерализацию или дубликатуру. Несмотря на многочисленные косвенные данные в пользу ретрокавального мочеточника, окончательный диагноз можно поставить только при лапаротомии путем визуализации непосредственного взаимодействия каудальной полой вены и одного из мочеточников.
Заключение
Для нас диагноз «ретрокавальный мочеточник» является редкой клинической ситуацией. В то же время, по статистике наших иностранных коллег, ретрокавальный мочеточник– достаточно частая находка при некропсии. Из этого следует вывод, что во многих случаях стеноз мочеточника на фоне аномалии воротной вены может протекать бессимптомно и быть случайным. Однако единственным возможным лечением данной патологии является хирургическое восстановление тока мочи по мочеточнику.
1. Berent A., Management of feline ureteral obstructions: an interventionalist’s approach. In: american College of Veterinary Surgery symposium Chicago, IL. USa, 2011.
2. Berent A., Weisse C., Bagley D. The use of a subcutaneous ureteral bypass for feline ureteral obstructions: 13 cases. World Congress Endourol. 2010.
3. Doust R.T., Clarke S.P., hammond G. et al. Circumcaval ureter associated with an intrahepatic portosystemic shunt in a dog. J am.Vet. Med. assoc. 2006; 228: 389–391.
4. Duconseille A.C., Louvet A., Lazard P. et al. Imaging diagnosis – left retrocaval ureter and transposition of the caudal vena cavain a dog. Vet Radiol Ultrasound. 2010; 51: 52–56.
5. Lingam K., Paterson P.J., Lingam M.K., Buckley J.F., Forrester a. Subcutaneous urinary diversion: an alternative to percutaneous nephrostomy. J Urol. 1994; 152: 70–2.
6. Salonia A., Maccagnano C., Lesma a. et al. Diagnosis and treatment of the circumcaval ureter. In: European urology supplements 5. amsterdam: Elsevier BV, 2006; 449–462.
Источник