- Менингоэнцефалит
- Классификация поражений головного мозга кошек
- Этиология
- Симптомы менингоэнцефалита кошек
- Диагностика менингоэнцефалита кошек
- Не медикаментозное лечение менингоэнцефалита кошек
- Медикаментозное лечение менингоэнцефалита
- Профилактика менингоэнцефалита кошек
- Новообразования головного мозга у собак и кошек
- Токсоплазмоз — симптомы и лечение
- Определение болезни. Причины заболевания
- Этиология
- Эпидемиология
- Симптомы токсоплазмоза
- Патогенез токсоплазмоза
- Классификация и стадии развития токсоплазмоза
- Осложнения токсоплазмоза
- Диагностика токсоплазмоза
- Лабораторная диагностика:
- Дифференциальная диагностика
- Лечение токсоплазмоза
- Прогноз. Профилактика
Менингоэнцефалит
Менингоэнцефалит — воспаление оболочек и вещества головного мозга. Заболевание характеризуется расстройством функций коры, подкорковых и вегетативных центров. Изолированное воспаление мозговых оболочек называется менингитом, воспаление вещества мозга – энцефалитом. В большинстве случаев регистрируется одновременное поражение вещества мозга и оболочек.
Классификация поражений головного мозга кошек
По происхождению:
По течению:
По характеру поражения:
При одновременном поражении головного и спинного мозга заболевание носит название менингоэнцефаломиелит.
Этиология
Поражение головного и спинного мозга кошек является осложнением при некоторых бактериальных и вирусных инфекциях (чуме кошек, болезни Ауески, бешенстве, лептоспирозе и листериозе), а также вследствие проникающих травм черепа, абсцедирования. Иногда оно происходит в результате микозов, миграции личинок аскарид, хирургическом сепсисе, распространении воспаления по продолжению со стороны спинного мозга, пневмониях. Предрасполагают к заболеванию ушибы, контузии и переохлаждение головы.
Симптомы менингоэнцефалита кошек
Клиническое проявление болезни разнообразно и обусловлено степенью поражения мозговых оболочек и мозгового вещества. В начальных стадиях менингоэнцефалита при преимущественном поражении оболочек мозга обычно наблюдают общие неспецифические признаки нарушения центральной и вегетативной нервной системы: повышение температуры тела до 40°С и выше, расширение зрачков, ограниченную подвижность глазного яблока, появление клонических судорог, ригидность мышц затылка и шеи, гиперестезию кожи, обострение сухожильных рефлексов, усиленную потливость. В дальнейшем развиваются прогрессирующее угнетение, рвота, расстройство акта глотания, угасание и полная потеря рефлексов, нарушение координации движений, расстройства вегетативной регуляции сердечно-сосудистой, дыхательной и пищеварительной систем.
При поражении коры головного мозга в первые дни наблюдают возбуждение, беспокойство, безудержное стремление вперед, агрессивность, обостренную реакцию на световые и звуковые раздражители, судорожные сокращения мышц, ослабление условных рефлексов, животное начинает упираться головой в препятствия. В дальнейшем симптомы возбуждения и агрессивности сменяются угнетением, пониженной реакцией на окружающее, ослаблением слуха и зрения, нарушением координации движений, парезами и параличами конечностей. При поражении продолговатого мозга может наступить смерть от паралича дыхательного и сосудодвигательного центров.
При внедрении вируса чумы в клетки головного мозга проявляются возбуждение, парестезия, миоклонические судороги, эпилептические припадки. При более широком поражении спинномозговых структур развиваются явления пареза, иногда совмещающиеся с миоклоническими признаками. Ритмические подергивания могут сохраняться и во сне. Тик нижней челюсти с гиперсаливацией — классическое поражение, встречающееся у кошек с прогрессирующей полиэнцефаломацией височных долей головного мозга.
Воспалительный неврит глазного нерва характеризуется внезапным слиянием глазного дна с расширенным, не реагирующим на свет зрачком. Увеличение глазного яблока, характерные вкрапления и исчерченность блестящего рисунка глазного дна является результатом вирусных поражений.
Диагностика менингоэнцефалита кошек
Диагноз ставят на основании анамнеза, клинических признаков, результатов лабораторной диагностики мочи, фекалий, крови, вирусологического и бактериологического исследований. При исследовании спинномозговой жидкости отмечают повышенное содержание клеточных элементов (плеоцитоз) и белка с преобладанием глобулиновых фракций.
Не медикаментозное лечение менингоэнцефалита кошек
Животному обеспечивают полный покой в затемненном помещении, не допускают переохлаждения и перегревания. На время лечения выгул запрещён. Кормят любимым кормом малыми порциями, в рацион включают легкопереваримые каши, кисель, овощные супы с добавлением небольшого количества вареного говяжьего фарша или мяса. В питье добавляют отвары и настои лекарственных растений, дезинфицирующих веществ. Рацион обогащают всеми витаминами, поливитаминами и микроэлементами. При показаниях применяют искусственное кормление. Используются холодные примочки на голову.
Медикаментозное лечение менингоэнцефалита
Также врачи проводят комплексное медикаментозное лечение.
В острой стадии менингоэнцефалитов обязательно назначают антибиотики в максимальных дозировках: бициллин -5, бицилин -3, кобактан, фортум, цефтриаксон.
При менингоэнцефалитах, включая вирусные, проводят курс лечения внутривенными инъекциями гексаметилентетрамина с глюкозой.
Применяются антигистаминные средства с глюкокортикоидами —дексаметазоном, дексакелом, дексафортом , преднизолоном и др. Указанные вещества обладают выраженными противоаллергическим и противовоспалительным свойствами.
В качестве спазмолитических препаратов, снижающих внутричерепное давление, дают дибазол, а также некоторые диуретики — фуросемид, диакарб, манит.
Часто применяют различные иммуностимуляторы (иммуномодуляторы) — интерферон, циклоферон, камедон, анандин .
Профилактика менингоэнцефалита кошек
Профилактика заключается в своевременном лечении пациентов с проникающими ранениями головы и черепа, ушибами, травмами, соблюдении правил асептики при операциях на голове. Необходимо регулярно вакцинировать кошек против вирусных и инфекционных болезней, проводить ежеквартальную антигельминтную обработку домашних питомцев.
Источник
Новообразования головного мозга у собак и кошек
Об опухолях головного мозга у собак и кошек – частоте их возникновения, вопросах диагностики и лечения, мы поговорили со старшим хирургом, неврологом «Биоконтроля», Николаем Александровичем Глазовым.
– Николай Александрович, насколько этот диагноз актуален для «Биоконтроля»?
– Вопрос неоплазии головного мозга достаточно актуален, особенно учитывая специфику нашей клиники. В месяц к нам поступают как минимум два-три пациента с таким диагнозом. Хотя встречаемость данной патологии не велика. У собак порядка 14,5 случаев на 100 000 (или 3 % от общего числа всех неоплазий), у кошек 3,5 случаев на 100 000 (или 2-3 % от общего числа всех неоплазий). Если говорить про новообразования нервной системы в общем, то головной мозг — наиболее уязвимое место. Поражение этого отдела мы (как и наши западные коллеги) встречаем чаще, по сравнению с другими отделами нервной системы.
– Можно ли говорить о породной или возрастной предрасположенности у кошек и собак?
– Опухолевое поражение головного мозга встречается у разных пород, независимо от возраста. Но по данным научной литературы в группу риска входят собаки старше пяти лет брахицефальных пород — боксеры, английские бульдоги и бостонские терьеры; и долихоцефалы – золотистые ретриверы. Из кошек – домашние короткошёрстные кошки. В среднем первичные симптомы у кошек владелец может наблюдать в 10-12 лет, а у собак в 8-10 лет.
– Как владелец может заподозрить наличие опухолевого процесса у своего питомца?
– Головной мозг – это достаточно пластичный орган. Если опухоль растёт медленно, то первые симптомы могут появиться только через несколько месяцев с момента зарождения образования. Выраженность клинических симптомов будет зависеть от локализации, степени и скорости роста. Наиболее распространённым клиническим признаком являются судороги. Они обычно ассоциируются с опухолями лобной доли (44%), обонятельной области (20%) и теменных долей (20%). Другие клинические признаки: хождение по кругу (23%), атаксия (шаткость походки) (21%), атаксия с повышенной чувствительностью шейного отдела. Во всех этих случаях необходимо обратиться за консультацией к неврологу. В ходе неврологического обследования врач может выявить нарушения в работе черепных нервов, изменение положения глазных яблок, потерю зрения, слуха, обоняния. А при внимательном сборе анамнеза и сам владелец укажет на то, что его питомец стал менее активным, перестал играть, осуществляет недостаточный груминг или поменял привычки.
– Что нужно сделать для подтверждения этого диагноза?
– Диагностировать неоплазию головного мозга без специального оборудования при жизни невозможно. Врач может только заподозрить наличие опухолевого процесса у пациента ориентируясь на анамнез и клинические признаки, но подтвердить эти догадки получится только после визуализации тканей головы, а в некоторых случаях только после взятия материала на гистологическое исследование. Но давайте по порядку.
После того, как у врача возникли подозрения на наличие неоплазии, он предложит владельцу провести либо МРТ, либо КТ головы. Сразу замечу, что МРТ наиболее чувствительный метод и даст расширенную информацию о состоянии тканей головного мозга. По ряду признаков часто можно сразу сказать, что животное имеет опухолевый рост. Но, к сожалению, не всегда. Существует ряд патологий головного мозга (чаще связанных с различными воспалениями), при которых полученные картинки лишь косвенно говорят о наличии объёмного поражения. В этих случаях может потребоваться анализ спинномозговой жидкости, что тоже, к сожалению, не всегда даёт однозначный ответ. Итоговым исследованием является гистологическое. Для его проведения необходимо получить кусочек подозрительного участка мозга, то есть провести операцию (трепанацию) и изъять данный материал. После проведения всех этих процедур на руках у врача и владельца будет точный диагноз, а именно: какой вид опухоли им предстоит лечить. Очень печально, но далеко не всегда все эти процедуры возможно выполнить.
– Расскажите, какие виды опухолей бывают?
– Неоплазии головного мозга делятся на первичные и вторичные. Первичные опухоли развиваются непосредственно из ткани мозга, его оболочек, эпителиальной выстилки желудочков и его сосудов. Вторичные опухоли развиваются из тканей, которые не являются частью головного мозга. Это могут быть как образования, растущие из костей черепа или воздухоносных путей, которые за счёт объёма и давления на ткани мозга нарушают его работу, так и метастатические поражения при первичном очаге совершенно в другой части тела (молочной железе, простате или лёгких).
Неоплазии головного мозга также делятся на злокачественные и доброкачественные. Но так как все они растут в ограниченном объёме (в полости черепа), то для здоровья больного, если их не удалить, это не столь принципиально.
У кошек и собак наиболее часто встречаются менингиомы и глиомы. Большинство первичных опухолей головного мозга являются одиночными. Отличительной чертой вышеописанных поражений является их медленный рост и локализация, что позволяет нейрохирургу разработать тактику вмешательства и выполнить её без спешки. И при этом, за счёт медикаментозной терапии, начинающейся ещё до вмешательства, практически полностью восстановить пациента.
Вторичные поражения ткани мозга вызывают более быстрое развитие симптомов. При наличии метастатического поражения сложно значительно улучшить состояние больного. При давлении на мозг изменёнными костями черепа улучшить самочувствие получится, как правило, только после их удаления.
– Какие методы лечения есть в арсенале ветеринарного специалиста?
– Существует два подхода: паллиативный и радикальный. Паллиативная терапия позволяет уменьшить влияние опухоли на ткань мозга в процессе роста: убрать отёк, а как следствие снизить давление на различные отделы мозга. В результате чего нередко удаётся убрать все симптомы, вызываемые опухолью (судороги, атаксию, агрессию и апатию). Для её проведения используется как внутривенное введение препаратов, так и пероральное (дача таблеток). При хорошем ответе на лечение можно значительно продлить качественную жизнь пациента.
Радикальное лечение заключается в проведении хирургической операции, в ходе которой происходит удаление образования. Как правило, в ветеринарии речь идёт о циторедукции, то есть определённое количество клеток или часть опухоли остаётся. Данный метод позволяет получить материал для гистологического исследования, на основании которого будет определён вид опухоли, что позволит врачу-онкологу рекомендовать дополнительные методы лечения.
Доступным вариантом лечения является лучевая терапия. Она позволяет уменьшить количество опухолевых клеток и замедлить рост опухоли. Наилучший эффект достигается после проведения хирургического лечения.
Химиотерапия используется очень ограниченно, так как химиопрепараты плохо проникают в поражённую ткань головного мозга. В ряде случаев она эффективна при лечении лимфомы центральной нервной системы.
– Что вы можете сказать о прогнозах для таких пациентов?
– При паллиативной терапии прогноз менее благоприятен: от одного до шести месяцев с момента возникновения симптомов. При хирургическом лечении – от полугода до двух-трёх лет жизни. Не забывайте, что возможны рецидивы. Часто после операции приходится принимать противосудорожные препараты пожизненно. Не исключена возможность развития менингоэнцефалита, который тоже придётся лечить.
При сочетанном использовании хирургического вмешательства и лучевой терапии прогноз наиболее благоприятный: от шестнадцати месяцев до трёх лет.
Источник
Токсоплазмоз — симптомы и лечение
Что такое токсоплазмоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 13 лет.
Определение болезни. Причины заболевания
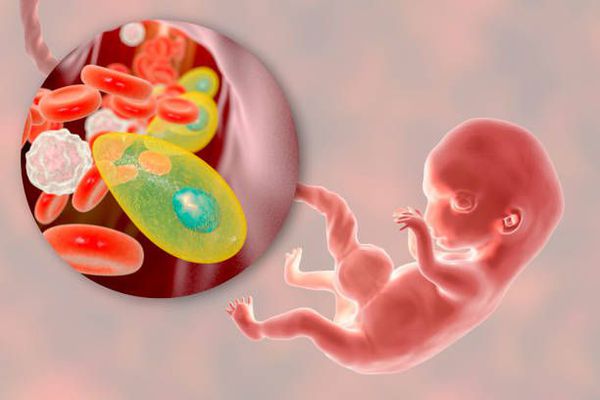
Токсоплазмоз — это острое и хроническое паразитарное заболевание человека в виде манифестных форм или носительства, вызываемое простейшими внутриклеточными паразитами — токсоплазмами, которые попадая в организм человека могут при условиях иммунодефицита поражать нервную ткань, среды глаза, сердечно-сосудистую и ретикулоэндотелиальную системы, вызывая поражение организма той или иной степени тяжести. Болезнь относится к группе TORCH-комплекса, т. е. вызывает врождённую патологию.
Этиология
- 1908 год: французские учёные Ch. Nicolle и L. Manceaux выявили у грызунов микроорганизм, получивший родовое название Toxoplasma (в пер. с франц. taxon — дуга, plasmon — форма) и видовое — gondii (по названию грызунов).
- 1923 год: чешский офтальмолог I. Yanku установил роль токсоплазмы в патологии человека, описав симптомы врождённого токсоплазмоза у погибшего ребёнка и выделив паразита из сетчатки глаза.
- 1938-1939 год: американские исследователи доказали возможность передачи инфекции от матери к плоду через плаценту и прижизненно выделили паразитов от больного ребёнка.
Таксономия:
Вид — Toxoplasma gondii
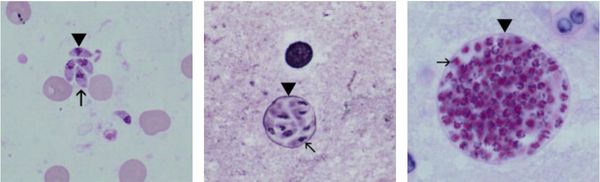
Токсоплазмы обитают в мире в трёх формах:
- трофозоиты (тахизоиты);
- цисты (брадизоиты);
- ооцисты.
Трофозоиты достигают 4-7 мкм в длину и 2-4 мкм в ширину. Их тело по форме напоминает полумесяц с заострённым передним и закруглённым задним концами, состоит из пелликулы (покровной ткани) и различных органелл. Такие паразиты обитают во всех клетках млекопитающих кроме эритроцитов, размножаются путём деления. Могут создавать движение, активно проникая в клетки хозяина через клеточную мембрану или посредством фагоцитоза (захвата и переваривания клетки). Обнаруживаются в тканях в острой стадии инфекции. Их скопление внутри одной клетки называют псевдоцистой. Трофозоиты неустойчивы вне клетки и во внешней среде, быстро погибают при высушивании, прогревании и применении дезинфицирующих средств. Хорошо окрашиваются по Романовскому. Чувствительны к различным химиопрепаратам (сульфаниламидам, некоторым макролидам и другим).
Цисты размерами до 100 мкм отличаются плотной оболочкой, через которую не могут проникнуть антитела или лекарственные препараты. Внутри оболочки сосредоточено 3000-5000 паразитов, со временем они увеличиваются. Цисты формируются в организме хозяина (в основном в скелетных мышцах, миокарде и ЦНС) и живут там десятки лет. Чрезвычайно устойчивы к воздействиям внешних факторов. При адекватной иммунной системе могут пожизненно находиться в состоянии функционального покоя и не приносить никакого вреда организму человека.
Ооцисты играют основную роль в передаче инфекции. Они представляют собой овальные образования 10-12 мкм в диаметре. Их развитие и формирование длится 3-24 дня и проходит в слизистой оболочке тонкой кишки кошек. Затем в течение 7-20 дней паразиты выделяются с испражнениями, после этого срока новые фекалии кошки уже не заразны. За сутки с испражнениях животного выделяется до 10 миллионов ооцист. Спустя 2-3 дня при температуре 24 °C происходит споруляция ооцист — образование спор. При благоприятных условиях микроорганизмы сохраняются во внешней среде до года и дольше.
Существует множество штаммов токсоплазм, одни из которых отличаются высокой вирулентностью, а другие относительно маловирулентны. [1] [2] [7] [9]
Эпидемиология
Учитывая большое количество латентных форм, заболевание не поддаётся общему исчислению — им может быть заражено не менее 1,5 миллиардов человек. Только ежегодно регистрируется около 200 тысяч случаев внутриутробного инфицирования.
Распространение возбудителя повсеместное — токсоплазма обнаружена на всех материках. После заражения паразиты способны пожизненно сохранятся в организме большинства животных и птиц. Количество случаев приобретённого токсоплазмоза в разных странах колеблется: от 85 % во Франции и Мадагаскаре до 15 % в США и Англии.
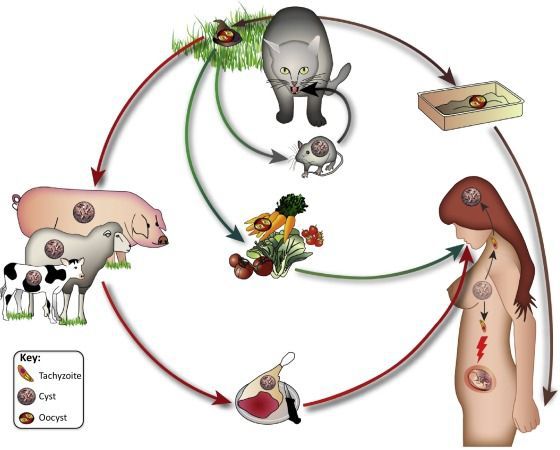
- Фекально-оральный:
- водный и пищевой путь — при недостаточной термической обработке, чаще при употреблении сырого мяса и фарша;
- контактно-бытовой путь — при несоблюдении санитарных норм в повседневной жизни, например, при общении с кошками.
- Вертикальный путь (от матери к плоду) — преимущественно при первичном заражении матери во время беременности, часто у ВИЧ-инфицированных в стадии СПИДа.
- Артифициальный путь — при пересадке органов, в которых расположены цисты, пациенту с плохим иммунитету.
- Аэрогенный путь — при попадании инфицированной ооцистами пыли в рот человека.
- Контактный путь — при повреждении целостности кожных покровов. Встречается крайне редко, в основном у работников лабораторий и скотобоен, отмечен лишь в некоторых источниках, явного практического значения не имеет.
От человека к человеку заболевание не предаётся (кроме случаев каннибализма). Нельзя заразиться посредством укуса насекомых и при половом контакте.
Инфицирование токсоплазмой вызывает устойчивый пожизненный иммунитет к повторному заражению, однако известны случаи рецидива первичной инфекции при заражении другим высоковирулентным штаммом (у беременных, заразившихся при употреблении сырого мяса с другого континента). [1] [3] [5] [8] [9]
Симптомы токсоплазмоза
Инкубационный период при манифестных формах (явных проявлениях болезни) длится от двух недель до двух месяцев.
Специфичных симптомов, характерных именно для токсоплазмоза, не существует.
В большинстве случаев приобретённого токсоплазмоза заболевание протекает бессимптомно или со стёртой клиникой, напоминающей нетяжёлое ОРЗ: кратковременная лихорадка, слабость, недомогание, повышение температуры до 38,0 °C, увеличение периферических лимфоузлов, небольшое увеличение печени и селезёнки.
Доказано, что токсоплазма может оказывать влияние на психику человека. Это выражается в учащении рискованных действий, снижении концентрации внимания, повышенной нервозности, у лиц с тяжёлым острым или длительным хроническим активным течением повышен риск развития шизофрении.
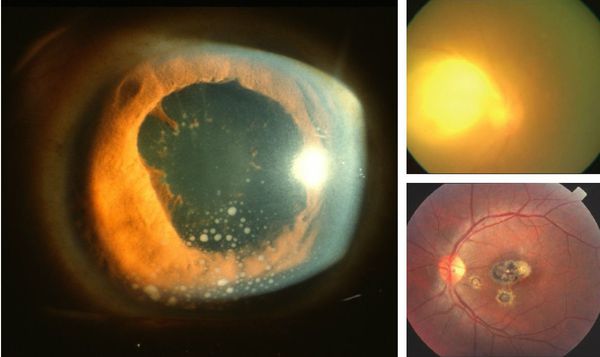
Иногда заболевание проявляется изолированной глазной формой — длительно текущие увеиты, иридоциклиты и хориоретиниты. Как правило, эти нарушения являются поздними проявлениями нераспознанного ранее врождённого процесса.
У людей с выраженным иммунодефицитом (ВИЧ, пересадка органов с последующей цитостатической терапией) возможно развитие генерализованного процесса с поражением нескольких органов (головного мозга, сердца, печени, почек, лёгких), нередко очень тяжёлого течения, проявляющегося в виде синдрома полиорганной недостаточности.
Токсоплазмоз у беременных может протекать в различных клинических вариантах и представляет опасность не столько для самой беременной (исключая тяжело протекающие патологии у беременных со СПИДом), сколько для плода.
При первичном заражении беременной токсоплазмозом имеет значение срок гестации:
- При инфицировании в первом триместре передача возбудителя плоду происходит лишь в 4 % случаев (к 13 неделе — в 6 %), но заканчивается, как правило, гибелью плода и выкидышем на ранних сроках. Если первичная инфекция у матери в первом триместре доказано, но выкидыш до 13 недели беременности не произошёл, то крайне высока вероятность, что внутриутробной передачи не было и ребёнок будет здоров.
- При инфицировании во втором триместре (особенно на 24-26 неделях) риск внутриутробной передачи резко возрастает и достигает 30-40 %, причём сопровождается развитием тяжёлых проявлений заболевания — одновременное увеличение селезёнки и печени, воспаление сосудистой оболочки и сетчатки глаза, поражения ЦНС в виде гидроцефалии, кальцификация, сыпь, миокардит, пневмония и другие.
- При заражении матери в третьем триместре передача инфекции ребёнку происходит с частотой до 90 %, однако проявления заболевания являются латентными или субклиническими и могут появиться спустя годы после рождения (отставание в развитии, нарушения зрения). [1][2][4][9]
Патогенез токсоплазмоза
Входные ворота токсоплазмоза — ротовая полость, оттуда ооцисты попадают в кишечник человека. Далее при развитии паразита (делении его клеток) образуются трофозоиты, которые мигрируют в различные органы и ткани (преимущественно в ЦНС и мышечную). В клетках они формируют псевдоцисты — большое количество размножающихся паразитов.
По мере развития и размножения токсоплазм поражённые клетки разрушаются, происходит заражение новых здоровых клеток, и при попадании возбудителя в кровоток паразиты разносятся по всему организму. Образуются некрозы с формированием фиброзной ткани и кальцификацией (отложение солей кальция в организме).
Под воздействием иммунитета безоболочечные трофозоиты превращаются в брадизоиты (оболочечные скопления токсоплазм), т.е. в тканевые цисты, которые сохраняются десятками лет в неактивном состоянии и при значительном снижении иммунитета способны к обратной трансформации с развитием обострения.
При первичной инфекции у беременных возбудитель проникает в ткани плода и вызывает воспалительный процесс, причём в разные периоды развития наблюдается различный характер воспаления: у эмбриона происходит лишь альтерация (дистрофия и некроз ткани без фиброза), в раннем фетальном периоде дополняется повышенным образованием соединительной ткани (фиброзом), а в позднем фетальном периоде присоединяется сосудистый компонент. Отсюда вытекают различные по характеру и тяжести поражения плода, которые зависят от сроков инфицирования матери. [1] [2]
Классификация и стадии развития токсоплазмоза
По течению процесса токсоплазмоз бывает:
- острым — до одного месяца;
- подострым — 1-3 месяц;
- хроническим — более трёх месяцев.
По клиническим признакам выделяют пять форм заболевания:
- Врождённый острый токсоплазмоз:
- манифестная форма (с указанием ведущих проявлений);
- субклиническая форма (с указанием способа верификации диагноза).
- Врождённый хронический токсоплазмоз:
- обострение / ремиссия;
- с резидуальными (остаточными) явлениями / без резидуальных явлений.
- Врождённый латентный токсоплазмоз.
- Приобретённый острый токсоплазмоз.
- Приобретённый хронический токсоплазмоз.
По степени тяжести заболевание бывает:
- лёгким;
- среднетяжёлым;
- тяжёлым (врождённая инфекция, токсоплазмоз при СПИДе).
По наличию осложнений выделяют:
- осложнённый токсоплазмоз;
- неосложнённый токсоплазмоз.
В Международной классификации болезней 10 пересмотра выделены шесть типов заболевания:
- B58.0 Токсоплазмозная окулопатия;
- B58.1 Токсоплазмозный гепатит (K77.0*);
- B58.2 Токсоплазмозный менингоэнцефалит (G05.2*);
- B58.3 Легочный токсоплазмоз (J17.3*);
- B58.8 Токсоплазмоз с поражением других органов;
- B58.9 Токсоплазмоз неуточнённый. [1][2][3]
Осложнения токсоплазмоза
При врождённой форме может возникнуть гидроцефалия, микроцефалия, задержка психомоторного развития и слепота. Эти осложнения сопровождаются увеличением или уменьшением размеров черепа, различными неврологическими расстройствами — косоглазием, судорогами, трудностью с сидением и держанием головы, рвотой и другими.
При глазной форме заболевания развивается слепота, снижение остроты зрения и воспалительные явления всех сред глаза. Причём возможно как рождение с грубыми дефектами зрения, так и появление воспалительных явлений и нарушения зрения спустя много лет после рождения.
Токсоплазмоз у иммунокомпрометированных людей осложняется шизофренией, токсоплазменный энцефалитом и полиорганной недостаточностью — тяжёлой патологией различных органов при выраженном иммунодефиците. При этом свойственна картина тяжёлого энцефалита. Прогноз, как правило, неблагоприятный. [1] [5] [8] [9]
Диагностика токсоплазмоза
Лабораторная диагностика:
- Клинический анализ крови: снижение уровня тромбоцитов, увеличение количества лимфоцитов и эозинофилов.
- Биохимический анализ крови: возможно повышение уровня трансаминаз и билирубина.
- Иммуноферментный анализ (ИФА):
- Выявление специфических антител класса M — острая инфекция или её реактивация. Имеет ряд недостатков — низкая специфичность, длительная циркуляция в организме, иногда до года после острого процесса. В сложных случаях уточнение следует производить при помощи метода «двойной сэндвич» или «иммунозахват» IgM ELISA.
- Выявление специфических антител класса G (клеток памяти) — носительство, инфицированность — появляются в среднем со второй недели заболевания и достигают пика на 1-2 месяце, сохраняются пожизненно, за исключением СПИД-ассоциированных заболеваний.
- Авидность IgG — уточнение давности заболевания. Недостатком является отсутствие стандартизации результатов, что зачастую приводит к различным ошибкам интерпретации. Наибольшее значение имеет высокая авидность, остальные результаты низкой и слабой авидности могут быть ошибочными и не должны трактоваться как недавно перенесённое заболевание при отсутствии других подтверждающих этот факт тестов.
- ПЦР-диагностика: выявление ДНК токсоплазмы в крови, других жидкостях и тканях человеческого организма. Особенно информативна в диагностике генерализованного, глазного и врождённого токсоплазмоза, в т. ч. в антенатальном периоде путём проведения амнио (не ранее 16 недель) и кордоцентеза (с 18 недели беременности).
- УЗИ-диагностика: внутриутробное выявление гидро- и микроцефалии, кальцификатов, гепатоспленомегалии и выраженной задержки развития. [1][2][4][5][6]
Дифференциальная диагностика
Токсоплазмоз — это инфекция с необычайно разнообразными проявлениями, поэтому ввиду неспецифичности проявлений основное место в дифференциальной диагностике отводиться лабораторному обследованию, а именно специфическим серологическим тестам.
Необходимо исключить следующие заболевания:
- инфекционный мононуклеоз (ВЭБ-инфекцию) — боли в горле, преимущественное увеличение затылочных и заднешейных лимфоузлов, характерные изменения гемограммы (появление большого количества атипичных мононуклеаров и отсутствие столь выраженных изменений при врождённом течении), положительные IgM и ПЦР крови;
- цитомегаловирусная инфекция — лимфоцитарный характер гемограммы, частое поражение слюнных желёз, положительные IgM, ПЦР крови;
- туберкулёз — длительное постепенное начало, лёгкий субфебрилитет (до 38,0 °C), ночная потливость, нездоровый румянец на щеках, кашель, специфические изменения в лёгких, положительные пробы на туберкулёз, выявление бациллы Коха в мокроте;
- лимфопролиферативные заболевания (лимфома Ходжкина, неходжкинские лимфомы) — специфические изменения при биопсии поражённой ткани (лимфоузлов);
- ВИЧ-инфекция — наличие факта возможного заражения, увеличение всех групп лимфоузлов, положительная серология;
- саркоидоз — специфические изменения в лёгких, положительные результаты гистологического исследования. [1][2][5]
Лечение токсоплазмоза
Большинство случаев приобретённого токсоплазмоза протекают в лёгкой или бессимптомной форме, они не регистрируются и, по-видимому, не нуждаются в каком-либо лечении.
Необходимость проведения специфической этиотропной терапии возникает лишь у некоторых групп пациентов:
- беременные с доказанным первичным инфицированием (в ряде случаев при реактивации хронической инфекции);
- дети с врождённой формой токсоплазмоза (при наличии явных клинических и лабораторных проявлений заболевания, субклинических и инаппарантных формах) — сроки и объём терапии зависят от конкретных данных;
- иммунокомпрометированные люди, у которых токсоплазмоз (острый или в фазе реактивации хронического процесса) протекает с выраженными клинико-лабораторными проявлениями. Основное направление воздействия в этом случае должно быть на устранение причины иммунодефицита, повышение уровня СД4 клеток.
Проведение лечения может осуществляться как в стационаре, так и амбулаторно в зависимости от выраженности процесса, реакции пациента на вводимые препараты, необходимости тех или иных вариантов патогенетического и симптоматического обеспечения. [1] [4] [7]
Прогноз. Профилактика
При приобретённом токсоплазмозе у иммунокомпетентных лиц прогноз благоприятный, у иммунокомпрометированных лиц (СПИД) прогноз серьёзен, нередки летальные исходы.
При врождённом токсоплазмозе исход заболевания зависит от сроков инфицирования плода:
- при инфицировании в первом триместре, как правило, происходит выкидыш;
- в более поздние сроки последствия варьируются от тяжёлых до резидуальных форм.
Основным методом профилактики приобретённого и врождённого токсоплазмоза является соблюдение санитарно-гигиенических правил, особенно беременными, не имеющими антител класса G к токсоплазмам:
- ограничение контакта с кошками;
- запрет на употребление сырого мяса, фарша и морепродуктов;
- тщательная промывка зелени, фруктов и овощей;
- мытьё рук перед едой;
- работа на приусадебном участке только в перчатках.
Для беременных особенно важен скрининг антител к токсоплазме, позволяющий выявить активно протекающее заболевание или риск его возникновения, а также вовремя провести медикаментозную профилактику острого токсоплазмоза беременной и снизить риск врождённой инфекции на 60 %. При отсутствии антител класса G в первом триместре необходимо отслеживать антитела IgM и IgG не только в тертьем, но и во втором триместре беременности.
В очаге токсоплазмоза противоэпидемические мероприятия не проводятся, вакцина на разработана. [2] [3]
Источник